Ce blog explore la manière dont les évaluations (Q)SAR pilotées par un protocole sont devenues courantes dans les évaluations d'impuretés basées sur l'ICH M7.
Application de l'ICH M7 : Étapes pratiques pour l'évaluation de la mutagénicité (Q)SAR
Neuf ans se sont écoulés depuis la publication des principes et procédures de mise en œuvre des analyses (Q)SAR recommandées parl'ICH M7.1un document que LeadscopeInstem) a contribué à initier et à promouvoir. Cette publication a joué un rôle important dans la manière dont les impuretés des médicaments sont évaluées à l'aide d'approches in silico. La publication, élaborée grâce à une collaboration interprofessionnelle, fournit des conseils pratiques sur la mise en œuvre des prédictions (Q)SAR, l'incorporation de l'examen des experts et la documentation des évaluations conformément à la ligne directrice ICH M72.
Cette première publication a ouvert la voie à un autre document essentiel3, axé sur la prise en charge des résultats indéterminés ou hors domaine, qui sont deux défis fréquemment rencontrés dans les évaluations réglementaires. Ensemble, ces documents ont jeté les bases d'une approche normalisée qui a été largement adoptée dans l'industrie et les flux de travail réglementaires. Il est à noter que ces deux documents sont en libre accès et ont été largement cités, notamment dans le document ICH M7 Q&A4, ce qui met en évidence leur pertinence et leur utilité constantes.
Outils d'aide à l'évaluation des classes ICH M7
L'impact de ces publications s'est étendu au-delà des publications écrites. Les principes et les flux de travail ont été mis en œuvre dans des outils logiciels5 qui soutiennent à la fois les évaluations internes de l'industrie et les soumissions réglementaires. Par exemple, la mise en œuvre du protocole ICH M7 de Leadscope intègre de multiples systèmes de prédiction (modèles statistiques QSAR, alertes d'experts) et des sources de bases de données dans un cadre décisionnel unifié et documenté pour dériver l'attribution de la classe M7 (figure16). Cette mise en œuvre rationalise le processus d'évaluation tout en soutenant l'examen des experts avec traçabilité.
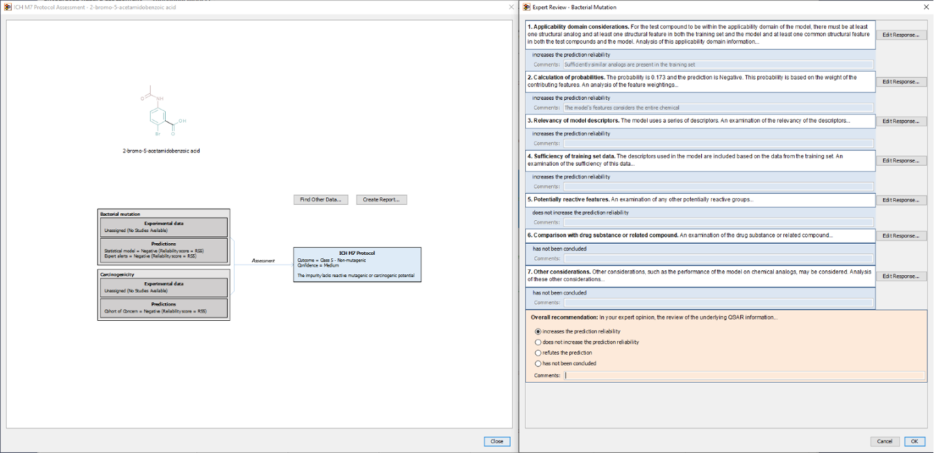
Figure 1 : Schéma décisionnel interactif ICH M7 résumant les résultats des QSAR et le cadre de l'examen par des experts
Procédures documentées pour d'autres paramètres
Il est important de noter que la mise en œuvre du protocole ICH M7 s'appuie sur le cadre plus large des protocoles de toxicologie in silico élaborés et publiés ces dernières années. Il s'agit notamment de flux de travail structurés similaires pour des paramètres tels que la toxicologie génétique7, la sensibilisation cutanée8 et l'activité endocrinienne9. Chaque protocole suit une architecture cohérente qui permet la transparence, la reproductibilité et l'intégration des résultats des modèles et des contributions des experts.
L'ICH M7 continue également d'influencer d'autres secteurs réglementaires, des approches similaires étant appliquées à l'évaluation des impuretés génotoxiques ou mutagènes dans les produits de santé animale10, les E&L et les résidus de pesticides11. En outre, les bases posées par les publications originales sur les principes et les procédures1,3 ont permis ces applications en démontrant comment les approches fondées sur des protocoles peuvent être à la fois scientifiquement rigoureuses et pratiques. Le développement d'outils fondés sur des protocoles a joué un rôle essentiel en garantissant que les évaluations sont non seulement scientifiquement solides, mais aussi cohérentes, efficaces et défendables, ce qui est important dans un environnement réglementaire.
Principaux enseignements:
- La ligne directrice ICH M72 a favorisé l'adoption de méthodologies normalisées pour l'évaluation du (Q)SAR.
- Des méthodologies normalisées1,3 ont été incorporées dans les protocoles (Q)SAR pour soutenir les évaluations d'impuretés (ICH M7) et d'autres cas d'utilisation d'une manière scientifiquement rigoureuse.
- La solution ICH M7 de Leadscope adhère aux principes et procédures établis décrits dans l'ICH M7 pour l'analyse des impuretés.
Vous pouvez accéder aux publications fondamentales et aux méthodologies normalisées pour la mise en œuvre des évaluations (Q)SAR dans le cadre de l'ICH M7 ici :
Principes et procédures pour la mise en œuvre des analyses (Q)SAR recommandées par l'ICH M7.
Références:
1. Amberg, A., et al, 2016. Principes et procédures pour la mise en œuvre des analyses (Q)SAR recommandées par l'ICH M7. Regul. Toxicol. Pharmacol. 77, 13-24. https://doi.org/10.1016/j.yrtph.2016.02.004
2. ICH, 2017. Directive ICH M7 (R1). Évaluation et contrôle des impuretés réactives à l'ADN (mutagènes) dans les produits pharmaceutiques afin de limiter le risque cancérogène potentiel (n° EMA/CHMP/ICH/83812/2013), ligne directrice harmonisée de l'ICH. Agence européenne des médicaments.
https://database.ich.org/sites/default/files/M7_R1_Guideline.pdf
3. A. Amberg et al, 2019, Principles and procedures for handling out-of-domain and indeterminate results as part of ICH M7 recommended (Q)SAR analyses, Regul. Toxicol. Pharmacol. 102, 53-64. https://doi.org/10.1016/j.yrtph.2018.12.007.
4. Ligne directrice ICH M7 : Évaluation et contrôle des impuretés réactives à l'ADN (mutagènes) dans les produits pharmaceutiques afin de limiter le risque cancérogène potentiel. Questions et réponses. https://www.ich.org/page/multidisciplinary-guidelines#7-3
6. Myatt, G. J., Bassan, A., Bower, D., Johnson, C., Miller, S., Pavan, M. et Cross, K. P. (2022). Implementation of in silico toxicology protocols within a visual and interactive hazard assessment platform (Mise en œuvre de protocoles de toxicologie in silico au sein d'une plateforme visuelle et interactive d'évaluation des risques). Computational Toxicology, 21, 100201. https://doi.org/https://doi.org/10.1016/j.comtox.2021.100201
7. Hasselgren, C., Ahlberg, E., Akahori, Y., Amberg, A., Anger, L. T. L. T., Atienzar, F., Auerbach, S., Beilke, L., Bellion, P., Benigni, R., Bercu, J., Booth, E. D. E. D., Bower, D., Brigo, A., Cammerer, Z., Cronin, M. T. D. M. T. D., Crooks, I., Cross, K. P. K. P., Custer, L., ... Myatt, G. J. G. J. (2019). Protocole de toxicologie génétique in silico. Toxicologie et pharmacologie réglementaires, 107. https://doi.org/10.1016/j.yrtph.2019.104403
8. Johnson, C., Ahlberg, E., Anger, L. T., Beilke, L., Benigni, R., Bercu, J., Bobst, S., Bower, D., Brigo, A., Campbell, S., Cronin, M. T. D., Crooks, I., Cross, K. P., Doktorova, T., Exner, T., Faulkner, D., Fearon, I. M., Fehr, M., Gad, S. C., ... Myatt, G. J. (2020). Skin sensitization in silico protocol. Regulatory Toxicology and Pharmacology, 116, 104688. https://doi.org/https://doi.org/10.1016/j.yrtph.2020.104688
9. Johnson, C., Marty, S., Kim, M., Crofton, K., Roncaglioni, A., Bassan, A., Barton-Maclaren, T., Domingues, A., Frericks, M., Karmaus, A., Kulkarni, S., Piparo, E. lo, Melching-Kollmuss, S., Tice, R., Woolley, D., & Cross, K. (2025). Un protocole in silico pour l'évaluation de l'activité endocrinienne : Integrating predictions, experimental evidence, and expert reviews across estrogen, androgen, thyroid, and steroidogenesis modalities. Computational Toxicology, 100364. https://doi.org/https://doi.org/10.1016/j.comtox.2025.100364
N'hésitez pas à nous contacter pour parler à un expert ou pour en savoir plus sur nos solutions ici.


