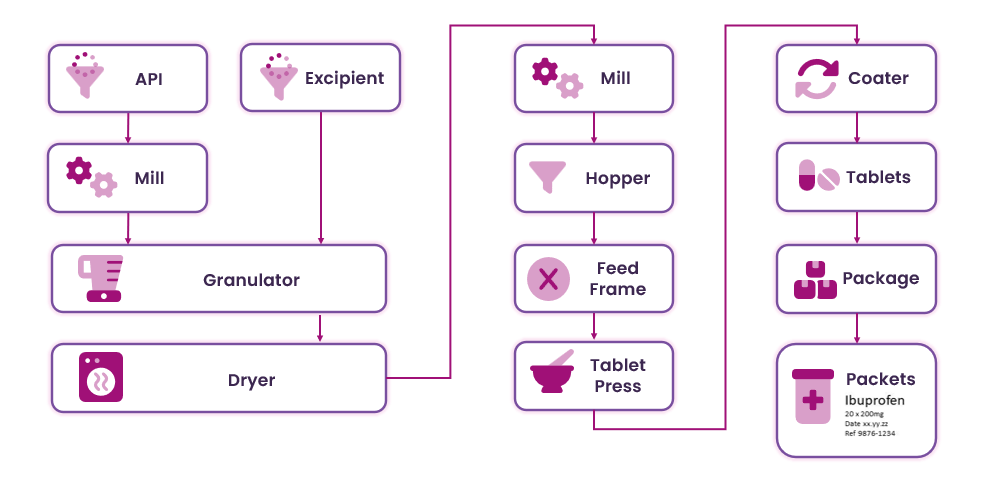
製造フローの特徴
自動車、パイプ、医療機器、医薬品を問わず、すべての製造工程は原材料から始まり、一連の工程を経て最終製品へと変化する。医薬品製造の場合、構成成分には通常、医薬品有効成分(API)、賦形剤、包装・表示材料が含まれる。例えば錠剤には、飲みやすくするためのコーティング剤や、他と区別するための着色剤が含まれることがある。
これらの錠剤は多くの場合、20個前後のブリスターパックに包装され、主要な消費者情報が印刷された段ボール箱に入れられる。自動車やアイスクリームの製造と同様、原薬からブリスターパックのホイルに至るまで、すべてのコンポーネントは、各サプライヤーから出荷されたバッチまでトレース可能でなければならない。同じ材料の複数のバッチを使用する場合、それぞれを製造記録の一部として文書化しなければならない。
重要なのはトレーサビリティで、製品の製造に使用されるすべての材料が、製造工程全体を通じて追跡可能であることを保証することである。
典型的な医薬品錠剤製造ラインの概要を図1に示す。調理と同様、様々な原材料の正確な比率は、原薬と賦形剤の必要量を定義したレシピによって管理される。原料は粉砕され、原薬の均一な分布を確保するために混合される。混合はスラリーまたはウェットミックスとして行われ、その後乾燥され、再度粉砕されて微粉末となる。このバルクパウダーは、打錠機を用いて錠剤に圧縮する前に、追加の賦形剤とブレンドすることができる。錠剤は必要に応じてコーティングされ、包装される。
試験は、原材料から最終包装製品に至るまで、プロセスの重要な各段階で実施される。例えば、入荷された原料は、使用に供される前にサプライヤーの仕様に適合していることを確認するために再試験されることがある。造粒機の出力を分析してAPIの均一な分布を確認し、粉砕された材料はAPIの比率と粒子の一貫性が正しく維持されていることを確認します。完成した錠剤のサンプルは、溶出試験、安定性試験、その他の品質保証試験のために保管される。
医薬品製造LIMSの要件
すべてのLIMSは、サンプルを追跡し、試験結果を関連付け、分析証明書(CofA)を作成し、バーコード化を使用し、バッチやサプライヤーなどの重要な情報とサンプルを関連付ける機能を必要とする。LIMSはまた、検査機器の校正と保守を管理し、各サンプル検査にどの機器が使用されたかを記録し、誰がそのサンプルを検査したか、その検査に適格であったかどうかを記録し、検査に使用される化学薬品と検査消耗品の在庫を管理する機能も含む。
しかし、典型的なQCサンプリングフローが個別のサンプルをモニターし、報告するのに対して、製造フローでは、より広範な情報を関連付け、管理および報告のために組み合わせる必要がある。製造フローでは、各製造バッチに投入される原材料と中間製品を管理するためのレシピ管理、フローの各部分(原材料、中間段階、最終製品)の試験結果を保管する機能、試験結果を原産原材料/供給業者および最終製品/顧客にリンクさせる機能、定義された限度内でプロセスを管理するための統計ツール、およびこれらのデータを迅速に検索して報告する機能を追加する必要がある。
医薬品製造LIMSの主要部分には以下が含まれる:
- 仕様管理
原材料(RM)、中間製品(IP)、最終製品(FP)の仕様を定義・管理し、必要な規格に準拠していることを確認する。 - レシピ管理
検証された処方に従って各製品を製造するために必要な成分と量を概説する。 - バッチ管理
製造工程を通してRM、IP、FPバッチを追跡・管理し、完全なトレーサビリティと管理を実現。 - Batch Genealogy
原材料と最終製品の関係を確立し、各製品にどのバッチが使用されたかの完全なトレーサビリティを可能にする。 - 製造サンプル管理
RM、IP、FP分析に必要な関連テストを含むバッチおよびサンプルテンプレートを定義する。 - 資材・在庫管理
製造中に採取された物理的サンプルや、実験室の消耗品、試薬、化学薬品の在庫を監視する。 - サプライヤー管理
材料、試薬、消耗品、原材料のサプライヤーに関する詳細な記録を管理し、コンプライアンスと監査準備をサポートする。 - 機器の較正とメンテナンス
検査機器の較正とメンテナンスをスケジュール、追跡、記録し、検証された適合機器のみが検査に使用されるようにする。 - コンピテンシーとトレーニングの管理
スタッフのトレーニングとコンピテンシーの記録を管理し、資格のある人材にタスクの割り当てを自動的に制限します。 - 試験法管理
分析試験法を整理・管理し、一貫性と規制遵守を確保する。 - CAPA(Corrective and Preventive Action)
是正処置と予防処置の体系的管理を通じて、継続的な品質向上を支援する。 - Skip Lot / Selective Testing
コンプライアンスを維持しながら効率を最適化するために、試験ルールの削減(例えば、5回連続でパスした後、20バッチごとに試験する)を実施します。 - ワークアサインメント
アナリストと機器を特定の検査に割り当て、作業負荷のバランスとリソースの最適利用を確保する。 - ランシート管理
ブランク、スタンダード、デュプリケートを含むサンプルのテストシーケンスを定義する分析ランシートを生成します。 - 機器統合
分析機器と直接接続してデータ転送を自動化し、手入力を減らして精度を向上。 - 外部ERPインターフェース
企業システム(SAPなど)とシームレスに統合し、検査計画やロットのインポート、バッチ使用決定や分析結果のエクスポートが可能。 - 製品の等級付け
試験結果と定義された品質基準に基づき、製品の等級付けや分類を容易にする。 - Chain of Custody(検体保管の連鎖)
検査プロセス全体を通じて、検体の保管場所、取扱者、状態など、検体の保管に関す る完全な記録を保持する。 - Certificate of Analysis (CoA) and Certificate of Conformance (CoC)
CoAとCoCの生成と管理を自動化し、規制当局への提出や顧客要件をサポートします。 - Advanced Analytics
製品の適合性、ラボのパフォーマンス、サプライヤーの信頼性、材料のばらつきに関する実用的な洞察を提供します。 - 安定性試験
安定性試験のワークフローを管理し、賞味期限を決定するための長期にわたる製品品質の保持を評価および文書化します。
シンプルさを追求
医薬品製造のワークフローは、一般的なQC LIMSフレームワークの上に構築された、さらに複雑なレイヤーを必要とします。これにより、バッチの作成から最終的な分析証明書(CoA)の交付まで、効果的な管理が保証されます。このバッチは、仕様とレシピの管理を通じて既知の再現可能な標準に従って製造され、定義されたサンプル管理手順に従ってテストされます。
受け入れ/拒否/再試験のゲーティングを伴う通常のサンプルテストはすべて不可欠であるが、原材料製品(RP)、工程内製品(IP)、完成品(FP)のバッチを追跡するという課題が加わった。これらは、リコールや監査が発生した場合に、どの原材料がどの製品バッチに使用されたかを正確に追跡できるような方法で関連付けられなければならない。このようなトレーサビリティは、FDA 21 CFR Part 11、EU Annex 11、ISO 17025、ISO 9001、およびcGxP規格への準拠が義務付けられている医薬品製造のような規制産業では、非常に重要な要件です。
定義済みのMatrix Gemini LIMS医薬品製造システムは、柔軟性を維持しながら、これらの厳しい規制要件を満たすように設計されています。Matrix Gemini LIMSが、コアソフトウェアにカスタムコードやHTMLの修正を必要としない設定可能なプラットフォーム上に構築されているのはそのためです。独自の設定ツールにより、ユーザーはプログラミングを変更することなく、スターターシステム内のワークフロー、画面、メニューを変更することができます。
この設計により、提供されるIQおよびOQスクリプトを使用して、スターターシステムの迅速な再検証が可能になります。その結果、大幅な時間の節約、迅速な実装、コストの削減が可能になり、製品をより効率的に市場に投入することができます。
このコンフィギュレーション・アプローチのもう1つの主な利点は、基盤となるソフトウェアが変更されないため、将来のアップグレードが簡素化され、新しい機能拡張や拡張が利用可能になったときに、その恩恵を受けることができることです。独自のコンフィギュレーションを管理したいユーザーには、3日間の包括的なトレーニングコースを提供しています。他の多くのLIMSベンダーとは異なり)サポート契約を無効にすることなく変更を加えることができ、サポートデスクに直接連絡し、必要に応じて特定の画面を共有して確認することもできます。
Matrix Gemini LIMSの強力な設定ツールは、製造LIMSにエッジを与え、効率を高め、コンプライアンスを維持し、ライフタイムコストを削減します。
これらの機能の多くはすべての製造業に適用できるため、Instem医薬品製造LIMSは、自動車、食品、電子機器、医薬品の製造にかかわらず、あらゆる製造環境に堅牢な基盤を提供します。
Matrix Gemini LIMSについての詳細、またはデモのご依頼は、こちらからお問い合わせください。


